FUENTE: BBC.
Parece la trama de una mala película de ciencia ficción: bebés humanos sacados del útero de sus madres y criados en cápsulas llenas de líquido.
Sin embargo, eso es exactamente lo que los científicos del Hospital Infantil de Filadelfia (CHOP), en Pensilvania (EE.UU.), proponen hacer para los bebés con riesgo de parto prematuro extremo.
Están desarrollando lo que denominan un «útero artificial» o, para ser más exactos, entorno extrauterino para el desarrollo del recién nacido (Extend).
El Extend no pretende hacer crecer un feto desde la concepción hasta el nacimiento, lo cual sería imposible aunque así se quisiera. Su objetivo es aumentar la tasa de supervivencia de los bebés extremadamente prematuros, los cuales se enfrentan a una gran cantidad de posibles efectos sobre su salud a lo largo de su vida.
Un embarazo sano normal dura unas 40 semanas y se considera que un bebé ha llegado a su desarrollo a las 37 semanas. Sin embargo, a veces surgen complicaciones en el embarazo que pueden hacer que el bebé tenga que nacer antes de tiempo.
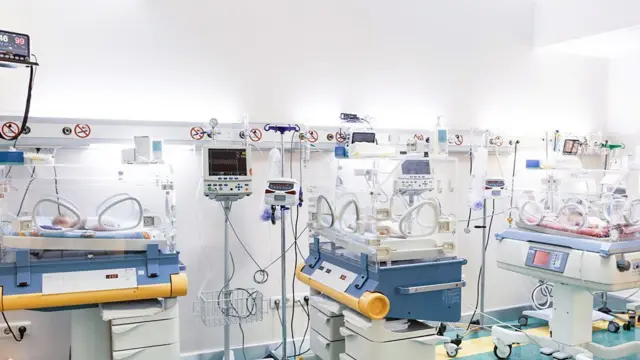
Por suerte, gracias a los enormes avances de la medicina neonatal en las últimas décadas, la mayoría de los bebés prematuros sobreviven y son dados de alta con pocas complicaciones. Los datos más recientes muestran que incluso el 30% de los bebés de 22 semanas de gestación sobreviven si reciben cuidados intensivos.
«Sinceramente, los bebés de 28 semanas e incluso los de 27 semanas están en general muy bien», dice Stephanie Kukora, neonatóloga del Hospital Infantil Mercy de Kansas City.
«Son realmente los bebés nacidos entre las 22 y 23 semanas los que presentan unos resultados tan graves que no estamos seguros de que la calidad de vida que alcanzen sea aceptable».
Riesgos de los prematuros
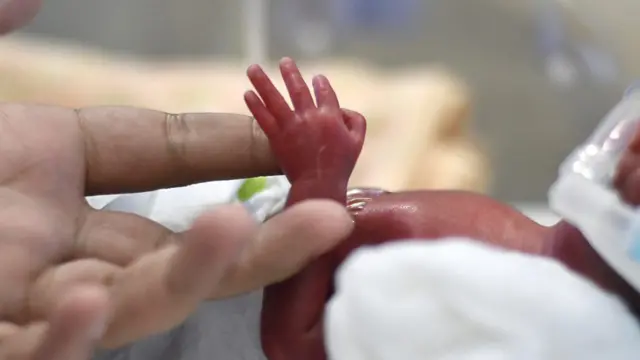
Los bebés nacidos en la cúspide de la viabilidad se enfrentan a menudo a graves problemas de salud.
Pesan menos de 900 gramos al nacer. Sus órganos críticos, como el corazón, los pulmones, los órganos digestivos y el cerebro aún no se han desarrollado lo suficiente como para mantenerlos con vida sin cuidados médicos intensivos.
Entre las complicaciones a corto plazo más frecuentes está la enterocolitis necrotizante (ECN), una enfermedad grave en la que los tejidos del intestino se inflaman y empiezan a morir.
Los bebés de esta edad también son muy propensos a las infecciones, la sepsis y el shock séptico, un descenso de la tensión arterial potencialmente mortal que puede dañar los pulmones, los riñones, el hígado y otros órganos.
Los problemas a largo plazo que pueden afectar a los bebés extremadamente prematuros incluyen parálisis cerebral, dificultades de aprendizaje de moderadas a graves, problemas de visión y audición, y asma.
¿Cómo ayudarlos?
La idea de los úteros y las placentas artificiales busca que los pulmones no entren en juego.
Actualmente, incluso la misma tecnología diseñada para salvar la vida de los bebés (oxígeno y ventilación) puede dañar sus frágiles pulmones.
«A esa temprana edad gestacional, los pulmones aún se están desarrollando y deberían estar llenos de líquido», afirma George Mychaliska, profesor de Cirugía, Obstetricia y Ginecología del Hospital Infantil C S Mott de la Universidad de Michigan.
«Pero cuando nacen muy prematuros, les colocamos un tubo endotraqueal en la tráquea y les metemos aire y oxígeno a alta tensión y presión en los pulmones. Está bien documentado que eso causa lesiones».
Con el tiempo, las lesiones provocan cicatrices en los pulmones y una afección conocida como displasia broncopulmonar o enfermedad pulmonar crónica. Los niños suelen abandonar el hospital con necesidad de oxígeno a largo plazo y ventilación mecánica para el resto de sus vidas.
La ventilación también puede aumentar el riesgo de ceguera retiniana. Los vasos sanguíneos que alimentan la retina del ojo no están completamente formados hasta cerca del nacimiento.
Demasiado oxígeno puede desencadenar el crecimiento de vasos sanguíneos nuevos y anormales, que a la larga pueden provocar un desprendimiento de retina.
Al eliminar los pulmones de la ecuación, la nueva tecnología permitiría que el feto pueda seguir desarrollándose en un entorno seguro hasta que el bebé esté listo para respirar por primera vez.
Hay tres grupos principales trabajando en esto.
Los tres se inspiran en una terapia ya existente llamada oxigenación por membrana extracorpórea (Ecmo), un tipo de soporte vital artificial que puede ayudar a una persona cuyos pulmones y corazón no funcionan correctamente.
En la Ecmo, la sangre se bombea fuera del cuerpo del paciente a una máquina que elimina el dióxido de carbono y añade oxígeno. A continuación, la sangre oxigenada se devuelve a los tejidos del cuerpo.
Este método permite que la sangre «eluda» el corazón y los pulmones, permitiendo que estos órganos descansen y se curen. Aunque la Ecmo puede usarse en bebés mayores, no es adecuado para bebés extremadamente prematuros. Los tres equipos intentan miniaturizar y adaptar la tecnología.
Sin embargo, existen sutiles diferencias entre los distintos dispositivos en desarrollo.
Las alternativas
Los científicos del Hospital Infantil de Filadelfia, dirigidos por el cirujano fetal Alan Flake, planean sumergir a los bebés prematuros en cápsulas llenas de líquido diseñadas para imitar el líquido amniótico del útero.
A continuación, los cirujanos conectarían los diminutos vasos sanguíneos del cordón umbilical del bebé a un dispositivo similar a la Ecmo. La sangre se bombea por el sistema utilizando el corazón del feto, igual que en la naturaleza.
En 2017, Flake y sus colegas tomaron ocho corderos prematuros de una edad gestacional equivalente a la de fetos humanos de entre 23 y 24 semanas y los mantuvieron vivos durante cuatro semanas utilizando el útero artificial.
Durante ese tiempo, los corderos parecieron desarrollarse con normalidad e incluso produjeron lana.
Por otra parte, el equipo de George Mychaliska, de la Universidad de Michigan, está desarrollando lo que llaman una placenta artificial.
En lugar de sumergir todo el feto en líquido, planean utilizar tubos respiratorios para llenar los pulmones del bebé con un líquido especialmente desarrollado. Su sistema drena la sangre del corazón a través de la yugular, de forma similar a las máquinas Ecmo tradicionales, pero devuelve la sangre oxigenada a través de la vena umbilical.
Los corderos prematuros mantenidos en la máquina sobrevivieron 16 días antes de ser transferidos con seguridad a ventilación mecánica
«Quería una plataforma que estuviera al alcance de la mayoría de los bebés y que pudiera utilizarse en las unidades de cuidados intensivos neonatales», explica Mychaliska.
«La tecnología no pretende sustituir las innumerables funciones de la placenta. Se centra en el intercambio gaseoso y en mantener la tensión arterial, la frecuencia cardiaca y la circulación fetal mientras los órganos prematuros están protegidos y siguen desarrollándose».
En un ensayo reciente de la placenta artificial, los corderos prematuros mantenidos en la máquina sobrevivieron 16 días antes de ser transferidos con seguridad a ventilación mecánica. Durante este tiempo, sus pulmones, cerebros y otros órganos siguieron desarrollándose bien.
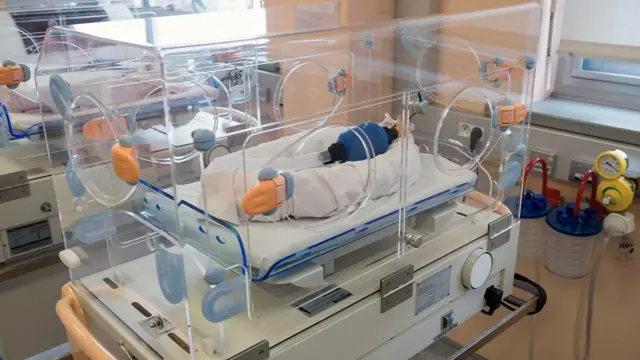
El tercer grupo, un equipo de Australia y Japón, está desarrollando un útero artificial denominado terapia de ambiente uterino ex vivo (Eve). Su objetivo es tratar a más fetos prematuros y enfermos que los otros dos grupos.
«Hemos llegado a un punto en el que podemos tomar un feto de 500 gramos y mantenerlo en lo que yo describiría como un estado fisiológico normal durante dos semanas», afirma Matt Kemp, catedrático de Obstetricia y Ginecología de la Universidad Nacional de Singapur, que dirige Eve.
«Es un logro bastante asombroso, pero por otro lado, el crecimiento de estos fetos es anormal».
La mayoría de los ensayos realizados con placentas o úteros artificiales se realizan con fetos de cordero que, por lo demás, están sanos y habrían llegado a su plena gestación si no se les hubiera interrumpido.
El problema es que los bebés extremadamente prematuros suelen nacer antes de tiempo debido a complicaciones de salud de la madre o del propio feto. Por lo tanto es más complicado tratarlos.
«En el único experimento que hemos hecho con fetos bastante comprometidos, esos animales son mucho más difíciles de tratar», dice Kemp.
«Creemos que está bastante claro que un feto muy pequeño no tiene la capacidad de dirigir su propio crecimiento de forma normal», explica.
«Su crecimiento es mucho más complicado y su presión y flujo sanguíneos son mucho, mucho más difíciles de mantener normales. Así que estamos avanzando, pero aún nos quedan muchas cosas por resolver».

En investigación todavía
¿Cuándo veremos placentas y úteros artificiales en los hospitales?
El CHOP es probablemente el centro que se encuentra más avanzado en el proceso de desarrollo. El equipo acaba de solicitar permiso a la Administración Federal de Medicamentos de EE.UU. para iniciar los ensayos de la Extend en humanos.
Mychaliska, por su parte, espera pasar a los ensayos clínicos en humanos en unos tres o cuatro años, después de que su equipo haya miniaturizado aún más su sistema para que pueda funcionar con los diminutos vasos sanguíneos de un neonato humano.
Sin embargo, Kemp sigue pensando que existen lagunas fundamentales en nuestros conocimientos sobre cómo crecen los fetos en úteros artificiales que es necesario subsanar antes de pasar a los ensayos.
«Creemos que está bastante claro que un feto muy pequeño no tiene capacidad para dirigir su propio crecimiento de forma normal, y eso se agrava cuando está enfermo», afirma Kemp.
«Intentamos desentrañar cómo interviene la placenta en los procesos normales de crecimiento. En eso estamos. Es una tarea bastante grande, por decirlo suavemente».
Cuestión de ética
También hay consideraciones éticas. En un artículo reciente, Stephanie Kukora argumenta que hay diferencias sutiles entre las distintas tecnologías que crean retos éticos únicos.
Por ejemplo, como los úteros artificiales de los equipos del EVE y el CHOP requieren la colocación de una cánula en el cordón umbilical, los bebés deben ser transferidos inmediatamente de la madre al dispositivo, ya que la arteria umbilical se cierra rápidamente tras el nacimiento.
Por tanto, las madres que hubieran podido dar a luz por vía vaginal tendrían que someterse a una cesárea temprana.
«Cuando se practica una cesárea tan pronto, no se puede hacer como se hace en su pleno desarrollo», dice Kukora.
«Implica una incisión que atraviesa la capa muscular del útero, y eso puede repercutir en futuros embarazos, lo que implica si pueden llegar a una gestación completa o si pueden tener un parto vaginal».

Hay más riesgos asociados a este procedimiento en comparación con un parto vaginal, lo que plantea cuestiones relacionadas con el consentimiento informado.
«Creo que una de las más importantes es cómo plantearemos a los futuros padres la realización de este ensayo», afirma Kukora.
«Podemos imaginarnos a unos padres que se enfrentan a una situación realmente triste, que acaban de recibir asesoramiento sobre los malos resultados a las 22 semanas, y que podrían estar realmente entusiasmados con algo nuevo aunque no se haya probado. Los padres hacen cualquier cosa por sus hijos».
Otro problema de transferir inmediatamente a un bebé al sistema Extend es que no hay oportunidad de evaluar cómo le habría ido con una terapia convencional.
«No se dispone de muchos datos, aparte de la edad gestacional, para decidir a quién se aplica el sistema Extend, porque el bebé aún no ha nacido y no se sabe cómo está», explica Mychaliska.
Esto puede significar que bebés que de otro modo habrían evolucionado bien con terapias tradicionales podrían ser tratados con una nueva tecnología no probada, cuyos riesgos están mucho menos cuantificados.
Sin embargo, Mychaliska cree que el Extend sería beneficioso para los bebés más prematuros, de 22-23 semanas de edad gestacional, que se sabe que sufren una elevada mortalidad y morbilidad.

Al drenar la sangre de la vena yugular en lugar de la arteria umbilical, los médicos tienen más tiempo para colocar a los bebés en la placenta artificial de Mychaliska.
Esto permite a los especialistas «estratificar el riesgo» de los bebés tras el nacimiento, con el objetivo de que solo los más enfermos sean transferidos a tratamiento con este método.
También se podría tratar primero a los bebés con terapia convencional y transferirlos posteriormente a la placenta artificial si no evolucionan bien. A diferencia de las otras dos tecnologías, las madres también pueden dar a luz por vía vaginal.
Sea cual sea la tecnología que primero llegue a los ensayos, es probable que los primeros participantes en ellos sean bebés nacidos antes de las 24 semanas que tengan muy pocas probabilidades de sobrevivir con un buen resultado utilizando el tratamiento convencional.
«Creo que la tecnología revolucionará el campo de la prematuridad y que la placenta artificial y Extend se complementarán en la práctica clínica», afirma Mychaliska.
«Pero tampoco está exenta de riesgos potenciales que deben evaluarse en un ensayo inicial de seguridad. Creo que la aplicación inicial de esta tecnología debería ser en bebés con pocas probabilidades de sobrevivir, y luego ampliarse a más prematuros una vez que determinemos los riesgos y la eficacia de esta tecnología.»
Si tienen éxito, las tres tecnologías ofrecerán una esperanza vital muy necesaria a los padres que inesperadamente entran en trabajo de parto prematuro.